Un monde d’éléments chimiques : enjeux sociétaux du Tableau périodique
PSL a mené en 2019 un projet de médiation scientifique collectif autour des éléments chimiques, pour célébrer le 150ème anniversaire du Tableau de Mendeleïev, avec le soutien de la Région Île-de-France. A cette occasion, les chercheurs de PSL et d’ailleurs ont présenté aux lycéens d’Île-de-France le rôle d’un ou plusieurs éléments chimiques dans l’Histoire de la planète, des arts et des sciences, et dans les grands enjeux de société auxquels nous faisons face en matière de santé, d’environnement et de gestion des ressources.
Le tableau périodique : un objet en constante évolution
François-Xavier Coudert (Chimie ParisTech - PSL, DIM Respore)
Le tableau périodique, qui semble si statique dans sa forme imprimée dans les livres scolaires, est un objet vivant ! Tout au long de l’histoire de la chimie, de nouveaux éléments ont été découverts. Lavoisier est le premier à dresser une liste exhaustive des éléments connus de son temps en 1789, puis Mendeleïev propose en 1869 de les arranger selon une classification en lignes et colonnes. Ce tableau porte son nom, même si tous les éléments présents aujourd’hui ne l’étaient pas à son époque.
Histoire du Tableau périodique : découvertes passées et à venir
Au XIXe siècle et au début du XXe siècle, le processus de découverte de nouveaux éléments consiste à isoler des éléments à partir de substances naturelles, notamment de minerais : par purification chimique, ou par passage d’un courant électrique — un procédé appelé électrolyse.
C’est à partir de 1940 que des éléments super-lourds, non présents dans la nature, sont créés par l’homme, par collision à haute énergie d’éléments plus légers. Une trentaine d’éléments super-lourds ont depuis été obtenus, dont le dernier est l’oganesson, qui porte le numéro 118. Cette recherche de nouveaux éléments continue au sein de plusieurs accélérateurs de particules dans le monde, en course pour synthétiser les éléments 119, 120 et suivants.
Le plomb dans l’histoire des arts et des techniques
Gilles Wallez (Chimie ParisTech - PSL / Sorbonne Université)
Dense, mou et terne… ces qualificatifs peu flatteurs sont souvent associés au plomb. En effet, bien que connu depuis l’Antiquité, celui-ci n’a jamais rivalisé avec les autres métaux dans les domaines qui leur sont habituellement dévolus. Il est aussi dit toxique, car l’asymétrie du cation Pb2+ le rend particulièrement nocif lorsqu’il se substitue à d’autres cations dans notre métabolisme.
Pourtant, le plomb n’en reste pas moins un métal utilisé de longue date pour sa facilité de mise en forme, comme dans les canalisations de la Rome antique et les vitraux des églises médiévales. Il est aussi l’élément de base des électrodes de la batterie « plomb-acide sulfurique » des automobiles à moteur thermique, quasiment inchangée depuis son invention en 1859 par Gaston Planté.
Le plomb a également marqué l’histoire des arts sous la forme de carbonates, plus connus sous le nom de « blanc de plomb », pigment utilisé depuis l’Antiquité égyptienne jusqu’au début du 20e siècle par tous les grands noms de la peinture, qui le tenaient pour le meilleur de tous les pigments blancs en raison de ses qualités physiques et chimiques. Ainsi Rembrandt l’utilisa-t-il pour élaborer ses célèbres clairs-obscurs, comme dans le Portrait de Maerten Soolsmans (1634).
Or et mines urbaines : recycler les éléments précieux de nos objets connectés
Anne Varenne (Chimie ParisTech – PSL)
L’or est un métal précieux connu depuis plus de 7000 ans, travaillé pour la fabrication d’objets de valeur et utilisé comme monnaie d’échange. Ce métal est l’élément chimique Au, du latin Aurum, et de numéro atomique 79. Il est extrait des sols par des procédés physiques et chimiques. Étant donné son exploitation actuelle exponentielle, les ressources naturelles en or seront épuisées d’ici 20 ans.
Les objets connectés, tels les téléphones portables, constituent des “mines urbaines” car leurs circuits imprimés sont riches en métaux précieux, l’or étant bien plus concentré (100 à 400 fois) dans ces déchets que dans un minerai issu des sols. Ainsi, l’extraction de l’or de ces mines urbaines est un enjeu stratégique et économique. Malheureusement, les procédés d’extraction de l’or des sols ne sont pas applicables à ces déchets, car leur conception complexe et employant différents matériaux (plastiques, céramiques, métaux divers) n’a pas été pensée pour une récupération sélective de chacun de ces composés. La recherche de nouvelles méthodologies d’extraction de ces métaux devenus stratégiques est donc cruciale.
Dans cette optique, notre laboratoire a montré l’efficacité d’un nouveau processus de séparation et de récupération de l’or à partir de déchets électriques et électroniques, développé dans un système miniaturisé peu impactant sur l’environnement.
Cobalt et lithium : les marchés influencent la disponibilité des ressources
Yves Jégourel (Université de Bordeaux)
La question de la disponibilité des ressources minérales, notamment du cobalt, est complexe. Le premier niveau d'analyse est géologique : il vise à identifier et à quantifier les ressources recherchées. En cas de succès, se pose une seconde question : dispose-t-on des capacités technologiques pour y accéder ?
Cette question de « l'accessibilité » doit par ailleurs intégrer trois autres niveaux d'analyse : politique, environnemental et sociétal. La ressource peut être disponible, accessible technologiquement, mais être localisée dans un pays dont le régime politique ne favorise guère l'accès à son sous-sol. L'extraction minière n'est par ailleurs pas neutre sur le plan environnemental et peut être contraire à la volonté des populations locales, raisons qui peuvent conduire à l'abandon d'un projet.
Le dernier niveau d'analyse est d'ordre économique. En effet, il y a derrière tout projet extractif une entreprise qui doit satisfaire à des objectifs de rentabilité. Si ceux-ci ne sont pas réalisables à long terme, le projet ne sera probablement pas mené à bien.
En ce sens, la disponibilité de la ressource dépend partiellement des prix, ce qui rend sa mesure plus complexe. Ainsi, une élévation des cours du cobalt, par exemple lors de tensions sur l’offre, aura tendance à favoriser le recyclage mais également à accroître les efforts de recherche pour remplacer cette ressource par d'autres, plus accessibles et moins coûteuses. L’offre augmente alors, tandis que la demande diminue, et, ainsi, la disponibilité de la ressource s'accroît.
Le calcium, de la biologie à l’histoire des sciences et des techniques
Didier Nectoux (Musée de minéralogie de Mines ParisTech – PSL)
Avec le calcium, il y en a pour tous les goûts. En biologie, cet élément est un composant essentiel des coquilles de mollusques ou des os des vertébrés. Les micro-organismes qui composent le plancton fixent aussi cet élément. Ils l’ont fait pendant des centaines de millions d’années. En s’accumulant dans les sédiments, une fois morts, ils ont contribué à former des masses considérables de calcaires composés de calcite, un carbonate de calcium. Ce sont ces mêmes calcaires qui, chauffés dans des fours à hautes température, permettent de fabriquer de la chaux et du ciment.
Par ses propriétés et caractéristiques, la calcite a aussi permis d’accéder à de grandes découvertes. Grâce à elle, au XVIIe siècle, Rasmus Bartholin a défini une propriété optique, la biréfringence (pour certains matériaux transparents, le fait de dédoubler un rayon lumineux qui les traverse). Un siècle plus tard, l’abbé René Just Haüy s’est appuyé sur l’observation de sa forme et de sa cassure pour développer une nouvelle science, la cristallographie (l’étude des cristaux à l’échelle de l’atome).
Enfin, le calcium, en s’associant avec le CO2 dissous dans l’eau pour former le calcaire, a, durant les ères géologiques, contribué à épurer l’atmosphère de ce gaz émis par une activité volcanique intense. Ce phénomène reste une piste à approfondir pour envisager un piégeage durable de ce gaz à effet de serre.
Enfants des étoiles : L’origine cosmique des éléments
Sylvie Cabrit (Observatoire de Paris – PSL / Sorbonne Université / DIM ACAV+)
Carbone, azote, oxygène : ces 3 atomes constituent (avec l’hydrogène) la majorité du poids de notre corps. C’est grâce à eux, et à une pincée d’oligo-éléments plus rares (calcium, magnésium, fer, iode, etc.), que nos cellules fonctionnent et que la vie est possible. Mais comment ces différents atomes se sont-ils formés ? Comment sont-ils apparus sur Terre ?
On pense souvent qu’ils sont là depuis la naissance de l’Univers. Et pourtant, non. Assembler plusieurs protons dans un même noyau exige des températures et densités très élevées qui n’ont subsisté que vingt minutes après le Big-Bang, tout juste assez pour former de l’hélium (et un peu de lithium). Il a fallu attendre 250 millions d’années pour que ces conditions se rencontrent à nouveau dans l’Univers, au cœur des étoiles. Celles-ci vivent en effet des millions, voire des milliards d’années, et ont ainsi le temps de synthétiser les éléments les plus légers (ceux qui se situent en haut du Tableau périodique), jusqu’au fer. Lors de leur mort, explosive ou lente, et de la fusion cataclysmique entre cadavres stellaires se produisent de nouvelles réactions nucléaires qui créent les éléments plus lourds du Tableau périodique, jusqu’à l’uranium.
Chaque atome de notre corps (à part l’hydrogène) est ainsi né dans une lointaine étoile qui l’a expulsé à sa mort dans l’espace interstellaire où, après un long voyage, il s’est déposé sur Terre à la formation du Système solaire… Nous sommes les enfants des étoiles !
Les métaux et la recherche contre le cancer
Mathilde Lepoitevin (ENS - PSL, DIM Respore)
Les solides poreux sont composés d’une structure solide et d’espaces vides, appelés pores (en savoir plus sur les solides poreux). Depuis une vingtaine d’années, un type de solides poreux hybrides apparaît prometteur, en particulier pour les applications biomédicales. Appelés Metal Organic Frameworks (MOF), ils présentent de nombreuses possibilités en matière de composition et de structure, notamment en raison de la variabilité de la taille des pores ou du volume poreux total.
Pour ces raisons, leur composition chimique peut être facilement ajustée. Cette grande polyvalence chimique, combinée à une grande diversité structurelle, offre une occasion unique de créer une bibliothèque de structures et de compositions. Parmi les applications que celles-ci permettent, l’absorption de différents gaz (on pense par exemple au gaz carbonique) ou leur séparation, mais aussi l'administration ciblée de médicaments et la détection de molécules.
En effet, leurs caractéristiques uniques font des MOF des candidats de choix pour des applications biomédicales. Par exemple, les nanovecteurs, enveloppes nanométriques qui transportent les molécules vers des cibles précises, doivent, dans les systèmes d'administration de médicaments, répondre à de nombreuses exigences pour être appliqués in vivo. Les MOF possèdent pour cela des propriétés avantageuses et ont ainsi été impliqués dans la conception de nanovecteurs pour la recherche contre le cancer.
Les éléments chimiques, entre technologies quotidiennes et gestion des ressources
Alain Fuchs (Université PSL)
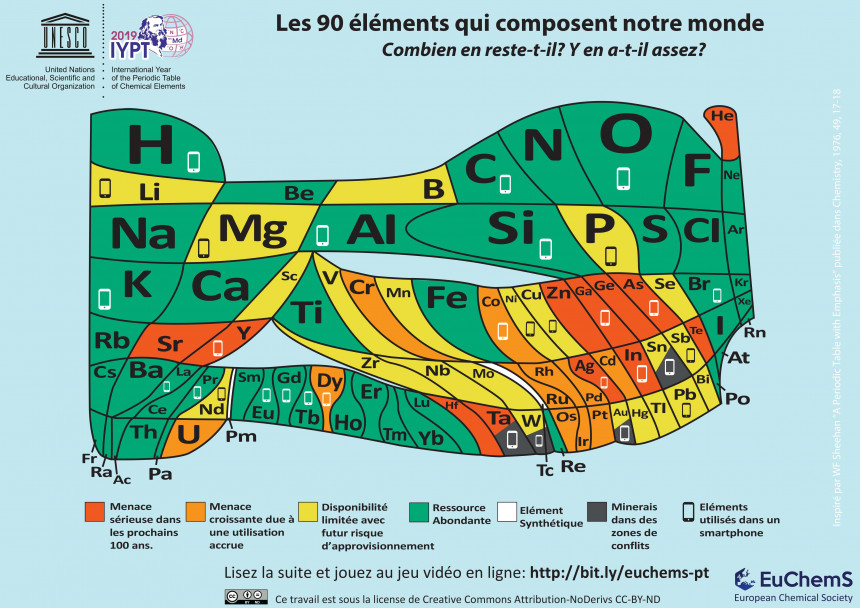
Combien d’éléments du tableau périodique trouve-t-on dans les objets de notre quotidien ? Environ 90. Et dans un smartphone ? Une trentaine d’éléments jouent un rôle crucial. Ces éléments ne sont pas tous aussi fréquents dans la nature ; certains sont courants (sodium, potassium, silicium, carbone) et d’autres sont rares (tellure, indium, etc.). On peut donc modifier le tableau périodique pour représenter chaque élément, non plus par une surface égale, mais en fonction de sa disponibilité.
Le tableau indique également les éléments qui sont extraits dans des zones de conflit, et pour lesquels l’approvisionnement peut devenir un problème géopolitique. Cette représentation du tableau permet de mieux réfléchir à la disponibilité des éléments, qu’elle soit limitée soit par leur faible abondance naturelle, soit par leur localisation, et doit nous inciter à mieux pouvoir les recycler. Avec 10 millions de smartphones jetés ou remplacés chaque mois rien qu’en Europe, la récupération et le recyclage des éléments est un enjeu crucial et un terrain d’innovation.
Retrouvez la version complète des mini-conférences.
Découvrez les Domaines d'Intérêt Majeur de la Région Île-de-France, Respore et ACAV+.